В области электрохимии вызванные изменения цвета в электролитах часто вызывают интерес и любопытство. Электролиты, играющие ключевую роль в составе аккумуляторов и различных электрохимических процессах, подвергаются изменениям, которые проявляются в изменении их цвета. Это явление, хотя и захватывающее, имеет свои корни в основополагающих принципах химии и физики. В данной статье мы рассмотрим причины изменения цвета электролитов и изучим основные механизмы, которые стоят за этим захватывающим явлением.
Понимание электролитов
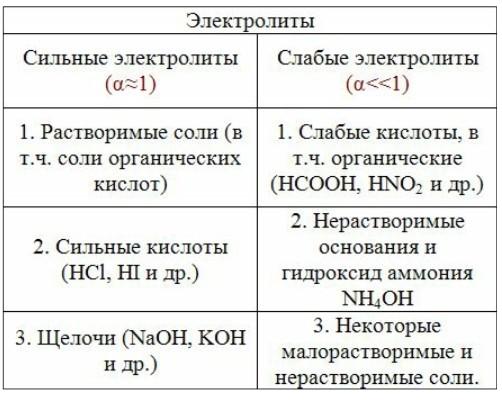
Электролиты представляют собой вещества, способные проводить электричество при растворении в обычно жидком растворителе. В контексте аккумуляторов электролиты играют ключевую роль, обеспечивая передачу ионов между катодом и анодом, что в свою очередь позволяет генерировать электрический ток. Обычно электролиты состоят из ионов, таких как катионы (положительно заряженные) и анионы (отрицательно заряженные), которые свободно перемещаются в растворе.
Цвет и поглощение света
Цвет вещества тесно связан с его молекулярной или ионной структурой. При взаимодействии света с материалом определенные длины волн поглощаются, в то время как другие проходят или отражаются. Тот цвет, который мы воспринимаем, представляет собой результат длин волн, которые не подвергаются поглощению и достигают наших глаз.
В случае электролитов изменения в цвете могут быть связаны с изменениями в электронной структуре растворенных ионов или молекул. Ионы переходных металлов, например, известны своей способностью поглощать определенные длины волн света, что приводит к появлению различных оттенков. В процессе электрохимических реакций окисление или восстановление этих ионов может вызывать сдвиги в их электронных конфигурациях, что приводит к заметным изменениям цвета.
Реакции окисления-восстановления
Многие электрохимические процессы основаны на окислительно-восстановительных (редокс) реакциях. В ходе этих реакций одно вещество подвергается окислению, теряя электроны, в то время как другое вещество приобретает электроны, подвергаясь восстановлению.

В случае электролитов эти окислительно-восстановительные реакции могут привести к изменениям в электронных конфигурациях присутствующих ионов, что влечет за собой изменение их спектров поглощения и, следовательно, цвета. В качестве примера рассмотрим литий-ионный аккумулятор. При перемещении ионов лития от анода к катоду во время разряда, литий подвергается окислению, отдавая электрон. Это изменение в электронной структуре может сказаться на цвете электролита, предоставляя визуальную индикацию электрохимических процессов, происходящих внутри батареи.
Химические изменения в электролите
Химические трансформации в электролите сыграть ключевую роль в формировании его цвета. Это явление обусловлено изменениями в электронной и молекулярной структуре растворенных ионов или молекул. Когда в электрохимической системе происходят окислительно-восстановительные реакции или другие химические превращения, состав электролита изменяется, что приводит к появлению новых химических соединений. Эти новые соединения часто обладают уникальными спектрами поглощения, влияющими на их взаимодействие с светом. Поглощение и отражение света определенных длин волн, следствие изменения молекулярной или ионной конфигурации, приводят к наблюдаемым изменениям цвета электролита. Ионы переходных металлов, часто присутствующие в электролитах, особенно предрасположены к выраженным цветовым проявлениям из-за их способности поглощать определенные длины волн. Таким образом, сложные химические изменения в электролите тесно связаны с динамичными изменениями его цвета, предоставляя исследователям и инженерам ценную информацию о состоянии и поведении электрохимической системы.
Заключение
В заключение важно отметить, что изменения в цвете, которые можно наблюдать в электролитах, могут быть результатом взаимодействия различных факторов, включая электронную структуру ионов, окислительно-восстановительные реакции и химические превращения. Эти изменения предоставляют ценное понимание динамической природы электрохимических процессов, служа визуальными индикаторами протекающих реакций в батареях и других системах. Глубокое понимание механизмов, лежащих в основе этих изменений в цвете, не только обогащает наши знания о тонкостях электрохимии, но также способствует разработке более эффективных и надежных электрохимических устройств.







